一种 基于225 Ac-DOTA 的新型预靶向放射免疫治疗 (PRIT) 系统已被证明可以在临床前环境中治愈高度致命的晚期腹膜内卵巢癌,且副作用极小。该疗法(抗 HER2 225 Ac-PRIT)针对卵巢癌中常见的 HER2 蛋白, 是治疗这种无法治愈的疾病的潜在疗法。这项研究发表在《 核医学杂志》九月号上。
上皮性卵巢癌是最致命的卵巢癌,经常表现为晚期疾病,例如腹膜癌病,其中疾病已扩散到整个腹膜腔。晚期疾病与不良预后相关,五年总生存率为 18% 至 46%。大多数患者因广泛的腹膜疾病负担和恶性肠梗阻而死亡。
“由于过去几十年来免疫和靶向疗法的爆炸式增长,特别是针对 HER2 的疗法,人们越来越关注替代性、更具创新性的疗法在治疗上皮性卵巢癌方面的潜在作用,”Sarah M. Cheal 博士说,纽约州威尔康奈尔医学院放射科分子成像创新研究所的教授。“在这项研究中,我们调整了 PRIT 系统以靶向上皮性卵巢癌中的 HER2,并探讨这是否可以有效治疗该疾病而没有明显的毒性。”
临床前研究包括五组,每组 8 至 10 只裸鼠,每组均携带腹膜癌瘤。两组小鼠接受一或两个周期的抗 HER2 225 Ac-PRIT 治疗;其他组接受替代治疗或不接受治疗,并用作对照组。每周监测体重和肿瘤进展长达 154 天。
肿瘤在未经治疗的小鼠中迅速扩散,导致中位生存期约为四个月。然而,当使用一或两个周期的抗 HER2 225 Ac-PRIT 治疗时,154 天后仍未达到中位生存期。研究结束时,抗 HER2 225 Ac-PRIT 治疗组中 75% 的小鼠被证实获得临床治愈。小鼠对所有治疗均耐受良好。
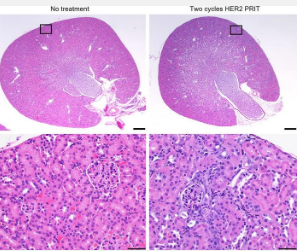
“在这项研究中,我们使用抗 HER2 225 Ac-PRIT 获得了高效力,同时保持了可接受的安全性。这些发现表明,当扩展到人类患者时,我们可以实现治疗性肿瘤辐射吸收剂量,而不会产生主要的正常器官毒性。”纽约纪念斯隆凯特琳癌症中心放射科的 Steven M. Larson 医学博士说道。
“此外,”纽约纪念斯隆凯特琳癌症中心儿科医学博士、哲学博士 Nai-Kong V. Cheung 表示,“由于基于 DOTA 的 PRIT 是模块化的,因此它可以适应其他癌症和下一代 PRIT使用 SADA(自组装解组装抗体)具有在肿瘤学中的隔室(例如腹膜)以及全身治疗诊断学中广泛应用的潜力。”
这项研究于 2023 年 6 月在线发布。
